西安交大科研人员在电热/热动力/化疗三模态协同治疗大肿瘤方面取得重要进展
恶性肿瘤是严重威胁人类健康的重大疾病,目前除传统的手术、放疗和化疗外,还建立了一系列肿瘤治疗新方法/策略,如生物治疗、免疫治疗、物理治疗(热、光、磁、电、超声)和动力学治疗等。但是由于肿瘤干细胞以及复杂的肿瘤微环境影响,中晚期治疗困难和复发等成为肿瘤治疗中难以克服的障碍。有研究发现肿瘤协同治疗效果明显优于单种治疗,如果将两种或多种不同方法(双模和多模态)结合起来协同治疗肿瘤,不仅疗效高(20天抑制瘤率超过90%)、毒副作用小,而且使用药量低、功能拓展性强。但是因为肿瘤复发和中晚期治疗困难,目前很少有协同治疗方法能够达到临床治疗的要求。为更接近临床肿瘤复发和中晚期治疗的现状,近来,研究人员将肿瘤在老鼠皮下长到300mm3以上形成大肿瘤模型,其体积大、生长旺盛,治疗难度更大,将肿瘤模型长时间(40-80天)观察其复发情况作为疗效的评判标准能更好地评价肿瘤协同治疗效果。
热动力疗法(Thermodynamic therapy,TDT)是近几年来发展起来的一种新型动力学治疗方法,其特点是利用热激活动力剂产生活性自由基杀灭肿瘤而不依赖于肿瘤的环境,目前主要使用的热动力剂是2,2'-偶氮双[2-(2-咪唑啉-2-基)丙烷]二盐酸盐(2,2’-azobis[2-(2-imidazolin-2-yl)propane] dihydrochloride,AIPH),该化合物热不稳定(半衰期温度是44°C)分解放出自由基,一般需要负载于载体上进入体内。常用的TDT加热方法有光和磁加热。而光热和磁热存在温度控制能力不够、温度分布不均匀等问题,难以满足TDT精准又均匀的加热需求。因此这些加热方法与热动力剂的匹配性不好,目前还没有专门用于热动力治疗的加热系统。
西安交通大学吴道澄教授等针对肿瘤热/热动力控温要求,在多物理场仿真结果的指导下,利用微纳加工技术如激光刻蚀等,研发了一系列热动力治疗专门用微电热针,经过优化设计了一种单回路微电加热针,利用激光技术在中空针体壁打孔将导线引出形成回路(图1上)。该微电热针可在0.2-2 V的低电压下实现动物体内1分钟快速升温、发热位置可调整、能实现长时间精确发热控温,特别适用于肿瘤热疗/热动力治疗。动物实验表明在施加电压为0.24 V时,60 s内小鼠肿瘤部位温度从34.7 ℃升高至53.8 ℃,加热20 s肿瘤温度就达到50 ℃,加热2 min温度达到稳态,肿瘤最大温度约56 ℃(图1下),该微电热针已经获得国家专利授权。
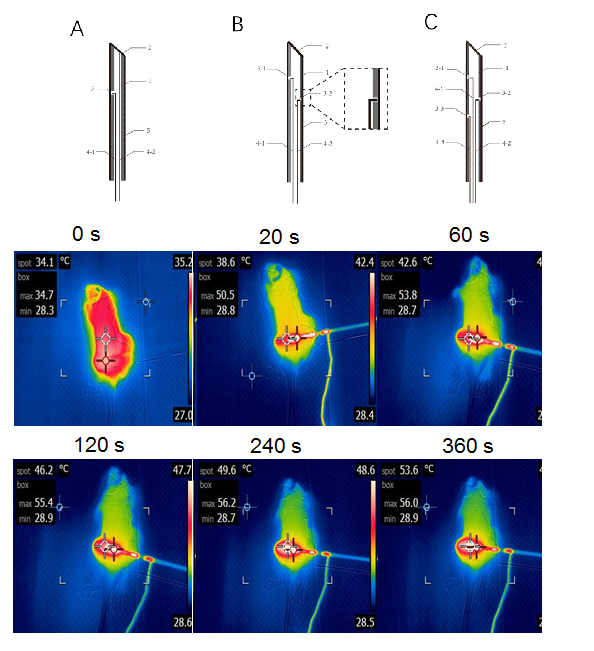
图1 微电热针的结构与性质
根据肿瘤热动力治疗的要求,课题组利用上述这种具有局部精确控温性能的微电热针(Micro-electrothermal needle,MEN)作为肿瘤热疗和热动力治疗的加热系统,该系统可以控制肿瘤部位温度在(T±7°C)20分钟以上。在此基础上提出了电热/热动力/化疗三模态协同治疗新策略。将化疗药物棉酚酮(Gn)、热力学试剂(2,2'-偶氮双[2-(2-咪唑啉-2-基)丙烷]二盐酸盐,AIPH)分子堆砌成纳米粒,其中掺杂少量聚乙烯醇和温敏相变材料月桂酸,再将肿瘤细胞膜修饰在表面形成分子堆积复合纳米粒子(APGn@MemNPs)(图2)。该复合纳米粒子尺寸为65±9.8nm,不仅载药量高、毒性低,还具有同源肿瘤靶向及热响应药物释放性能。
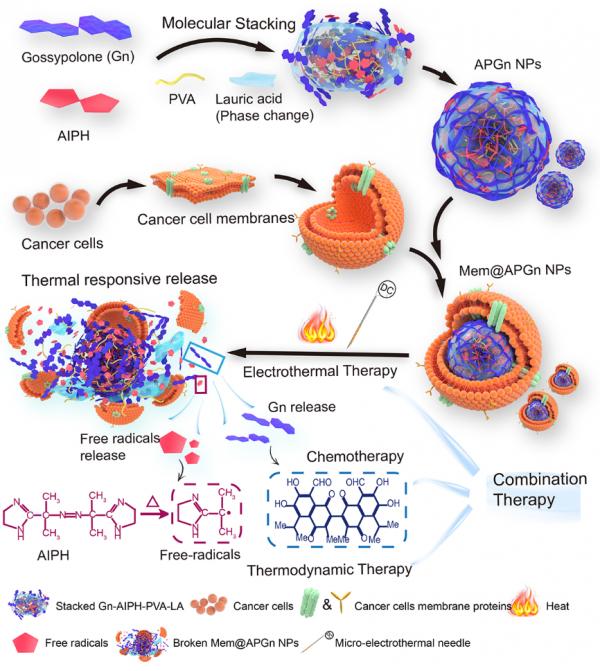
图2 大肿瘤电热/热动力/化疗三模态协同治疗
APGn@MemNPs进入体内后利用同源肿瘤细胞膜靶向到肿瘤部位,在微电热针加热下热疗的同时,月桂酸迅速相变释放AIPH,产生大量自由基杀灭肿瘤,而Gn的释放相对缓慢用于长期化疗。这种将短期电热/热力学治疗与长期化疗相结合的策略可以最大限度地发挥不同治疗方法的疗效,对于大肿瘤(≈300 mm3)综合治疗效果显著,实验表明该方法对大肿瘤模型16天抑瘤率为99.89%,60天肿瘤复发率仅有20%。综合疗效有较大的提高,该研究在未来的肿瘤治疗中具有广阔应用前景。
该研究成果日前以《棉酚酮和热力学剂分子堆积复合纳米颗粒电热-热动力-化疗三模态协同治疗小鼠大肿瘤》(Molecular Stacking Composite Nanoparticles of Gossypolone and Thermodynamic Agent for Elimination of Large Tumor in Mice via Electrothermal-Thermodynamic-Chemo Trimodal Combination Therapy)为题在国际著名学术期刊《先进功能材料》(Advanced Functional Materials)上在线发表,第一作者为西安交通大学生命学院博士生刘怡茗,吴道澄教授为唯一通讯作者,西安交通大学生物医学信息工程教育部重点实验室和生命学院为该论文的第一和唯一通讯作者单位。该研究成果是吴道澄教授课题组在无限配位聚合物联合化疗治疗肿瘤、肿瘤光热化疗和光热/无限配位聚合物双药协同肿瘤治疗之后的又一重要成果。
该工作得到了国家自然科学基金和国家重大科学仪器设备项目的资助。西安交通大学分析测试中心为本工作提供了大量测试表征支持。
论文链接:https://doi.org/10.1002/adfm.202201666
 千变万“化”展青春风采 笃志好“学”续精彩征途——西安交通大学第二届大学生化学实验创新设计大赛成功举办
千变万“化”展青春风采 笃志好“学”续精彩征途——西安交通大学第二届大学生化学实验创新设计大赛成功举办 传递生命力量 西电学子陈培积成功捐献造血干细胞
传递生命力量 西电学子陈培积成功捐献造血干细胞