西安交大科研人员发现隔日禁食改善肥胖和糖尿病等代谢综合症的线粒体机制
糖尿病被认为是“慢性癌症”,由饮食、环境、药物、遗传等因素导致的体内胰岛素分泌不足或机体敏感性降低而出现的血糖代谢紊乱,其中饮食失调导致的肥胖是糖尿病的主要风险因素之一。近几年我国肥胖症和糖尿病患病率大幅上升,已然是全球糖尿病的的重灾区,最新发布的《2021IDF全球糖尿病地图(第10版)》显示,中国是世界糖尿病病人最多的国家。过去的10年间(2011年―2021年),我国糖尿病患者人数由9000万增加至1.4亿,增幅达56%,而预估我国糖尿病和糖尿病前期总患病率已经达到50.5%(JAMA, 2021)。尽管糖尿病的临床治疗已日趋规范,但有限的靶向药物及普遍存在的环境、生活风险因素使得疾病治疗率和空置率较低。为此,运动、热量限制、饮食限制等多种生活方式的干预治疗研究迅速成为近年来糖尿病基础科研和临床治疗领域所关注的重点方向。
隔日禁食是一种新型的生活干预方式,即24小时禁食,24小时随意进食循环进行的生活模式,备受领域内科学家的关注。尤其在2019年,奥地利科学家利用衰老人群进行长达6个月的隔日禁食干预,发现隔日禁食可以安全且有效地改善衰老症状,提高代谢健康(Cell Metabolism, 2019),这一临床研究使得隔日禁食获得前所未有的关注。但隔日禁食如何实现机体代谢能力的改善,具体发生机制仍未解析,这一科学内容的探讨将可能在糖尿病临床干预、靶向药物研发等方面获得创新性成果。
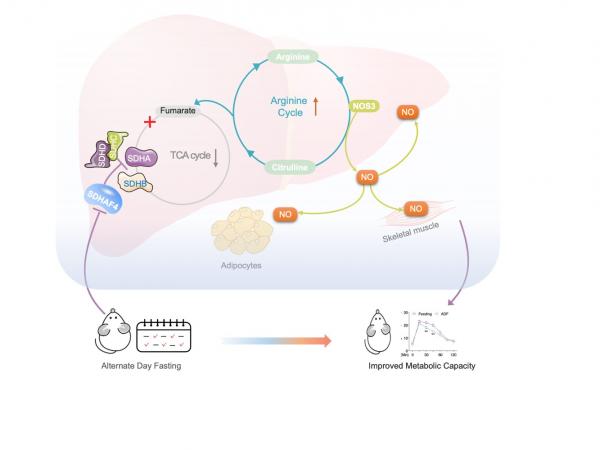
为此,生命学院刘健康教授与前沿科学技术研究院冯智辉教授与合作,利用多种基因敲除小鼠,结合隔日禁食模型、高脂饮食模型,通过多组学联合分析、线粒体稳态综合检测、组织细胞共培养、代谢行为学系统分析等多种实验手段,成功解析了隔日禁食改善机体代谢敏感性的具体机制。团队发现,隔日禁食可以通过抑制肝脏线粒体复合物II动态组装,激活肝细胞内精氨酸/一氧化氮代谢网络,通过向肝细胞外释放一氧化氮靶向提高脂肪、肌肉等重要靶器官的胰岛素敏感性,从而有效预防肥胖和改善糖尿病症状。这一研究不仅首次揭示隔日禁食的作用机制,为肥胖症和糖尿病防治研究提供全新靶点,更是革新了对线粒体功能生理病理调控的传统认知,具有重要的科学意义。
该研究成果以“肝脏线粒体复合物II组装停滞可驱动全身代谢能力的提升”(Hepatic Suppression of Mitochondrial Complex II Assembly
Drives Systemic Metabolic Benefits)为题,发表在权威科学期刊《先进科学》(Advanced Science,影响因子16.8)上。该工作是生命学院博士生王雪强、吕伟强、助理教授许洁等在冯智辉教授与刘健康教授共同指导下完成,同时获得前沿科学技术研究院邵永平教授、第二附属医院邹璇副研究员、生命学院龙建纲教授及上海交通大学张芳教授对该工作的多方面指导和支持。西安交通大学为论文的第一作者和通讯作者单位。该工作得到国家自然科学基金面上项目、重大专项、国家“973”项目等经费支持。这是冯智辉教授和刘健康教授团队继去年在发表了线粒体表观遗传学调控代谢综合征的里程碑式论文后的第二篇《先进科学》论文。
论文链接https://doi.org/10.1002/advs.202105587
 网信院开展“红色剧本+”党史校史学习活动
网信院开展“红色剧本+”党史校史学习活动 西电经管学子“经”心抗疫尽显担当
西电经管学子“经”心抗疫尽显担当